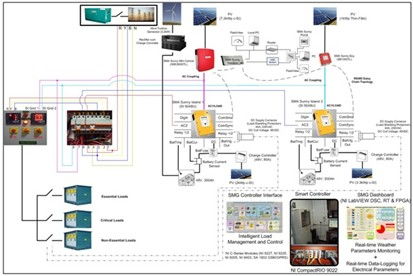
隨著能源結(jié)構(gòu)轉(zhuǎn)型和可再生能源的普及,分布式發(fā)電系統(tǒng)在電力供應中扮演著越來越重要的角色。美國國家儀器(NI)提供了一套高效的軟硬件平臺,其中NI CompactRIO作為強大的實時控制器,結(jié)合NI LabVIEW圖形化編程環(huán)境,為開發(fā)智能微電網(wǎng)系統(tǒng)提供了理想的解決方案。本文將探討如何利用這些工具進行軟件開發(fā),實現(xiàn)微電網(wǎng)的監(jiān)控、優(yōu)化和控制功能。
一、微電網(wǎng)系統(tǒng)概述與NI平臺優(yōu)勢
智能微電網(wǎng)系統(tǒng)整合了分布式發(fā)電資源(如太陽能、風能)、儲能設備和負載,通過智能控制實現(xiàn)能源的高效利用和電網(wǎng)穩(wěn)定性。NI CompactRIO結(jié)合了實時處理器、可重配置FPGA和模塊化I/O,能夠處理高速數(shù)據(jù)采集和復雜控制算法,而LabVIEW的直觀圖形化編程簡化了系統(tǒng)集成和調(diào)試過程。這種組合支持快速原型開發(fā)和部署,適用于研究機構(gòu)和工業(yè)應用。
二、軟件開發(fā)流程與關鍵組件
在開發(fā)基于NI CompactRIO和LabVIEW的微電網(wǎng)系統(tǒng)時,軟件設計通常遵循模塊化原則。使用LabVIEW創(chuàng)建數(shù)據(jù)采集模塊,通過CompactRIO的I/O模塊(如電壓、電流傳感器接口)實時監(jiān)控發(fā)電、儲能和負載數(shù)據(jù)。開發(fā)控制算法模塊,實現(xiàn)功率平衡、頻率調(diào)節(jié)和故障保護功能,利用LabVIEW的PID工具包和狀態(tài)機架構(gòu)提升響應速度。集成通信模塊(如Modbus、TCP/IP)支持與外部設備(如逆變器或電網(wǎng))的數(shù)據(jù)交換,并通過LabVIEW的Web服務功能實現(xiàn)遠程監(jiān)控和數(shù)據(jù)分析。
三、應用實例與效益分析
一個典型的應用案例是校園或工業(yè)園區(qū)的微電網(wǎng)系統(tǒng)。通過CompactRIO采集太陽能板輸出和電池狀態(tài),LabVIEW軟件進行實時優(yōu)化,動態(tài)調(diào)整能源分配以降低電網(wǎng)依賴。這種方案不僅提高了能源效率,還增強了系統(tǒng)的可靠性和可擴展性。使用NI平臺,開發(fā)周期縮短了30%以上,同時降低了硬件成本,得益于LabVIEW的復用性和CompactRIO的靈活性。
四、挑戰(zhàn)與未來展望
盡管NI工具簡化了開發(fā),但微電網(wǎng)系統(tǒng)仍面臨集成復雜性和實時性挑戰(zhàn)。未來,結(jié)合AI算法和云平臺,LabVIEW可以進一步擴展智能預測功能,實現(xiàn)更自主的能源管理。總體而言,NI CompactRIO和LabVIEW為分布式發(fā)電的智能微電網(wǎng)提供了強大支撐,推動可持續(xù)能源發(fā)展。